化學中考中,鹽和化肥是重要的考查內容,其相關的實驗探究題更是考察學生綜合能力的關鍵。本專題試題由一線名師精心整理,緊扣中考考點,旨在通過典型實驗題目,幫助學生掌握鹽的性質、化肥的鑒別與使用等核心知識,提升實驗探究與問題解決能力。
一、 核心知識梳理
1. 鹽的化學性質:
* 與某些金屬反應(金屬活動性順序的應用)。
- 與酸反應(生成新鹽和新酸)。
- 與堿反應(生成新鹽和新堿)。
- 與某些鹽反應(生成兩種新鹽)。
- 化肥的種類與作用:
- 氮肥:促進葉色濃綠,枝葉茂盛。
- 磷肥:促進根系發達,增強抗寒抗旱能力。
- 鉀肥:促進莖稈粗壯,增強抗病蟲害和抗倒伏能力。
- 復合肥料:同時含有兩種或兩種以上營養元素。
- 常見離子的檢驗:如Cl?、SO?2?、CO?2?、NH??等,這是鑒別鹽和化肥成分的基礎。
二、 精品試題精講(節選)
【例題1】(物質鑒別題)
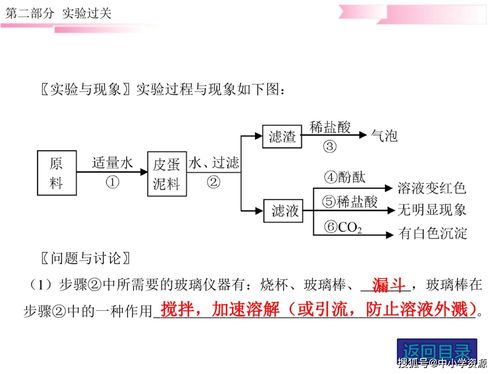
實驗室有四種白色固體,分別是碳酸鈉、硫酸鈉、氯化鈉和碳酸鈣,請設計實驗方案進行鑒別。
【參考答案與分析】
1. 物理方法:觀察溶解性。取少量樣品于試管中,加入足量水,振蕩。不溶解的是碳酸鈣。
2. 化學方法:
* 向三種溶液(或剩余固體加水后的上層清液)中分別滴加稀鹽酸。產生氣泡的是碳酸鈉溶液。
- 向剩余兩種溶液中分別滴加氯化鋇溶液(或硝酸鋇溶液),產生白色沉淀的是硫酸鈉溶液(生成BaSO?)。
- 無明顯現象的是氯化鈉溶液。
本題考點:鹽的溶解性、碳酸鹽與酸的反應、硫酸鹽的檢驗。
【例題2】(實驗探究題)
某農資商店有一包鉀肥標簽脫落,可能是氯化鉀、硫酸鉀或碳酸鉀。請設計實驗確定其成分。
【參考答案與分析】
1. 取少量樣品于試管中,加入足量稀鹽酸,若有氣泡產生,則原樣品為碳酸鉀。
2. 若無氣泡,則樣品為氯化鉀或硫酸鉀。另取樣品配成溶液,滴加幾滴硝酸鋇溶液,若產生白色沉淀(不溶于稀硝酸),則原樣品為硫酸鉀;若無明顯現象,則為氯化鉀。
本題考點:化肥種類鑒別、碳酸鹽與酸的反應、硫酸根離子的檢驗。
【例題3】(綜合應用題)
某同學在探究銨態氮肥(如NH?Cl)性質時,發現其與堿性物質混合會釋放出有刺激性氣味的氣體,導致肥效降低。請解釋原因,并寫出實驗室檢驗銨根離子(NH??)的方法。
【參考答案與分析】
原因:銨鹽能與堿反應生成氨氣(NH?),氨氣逸出導致氮元素流失。例如:2NH?Cl + Ca(OH)? → CaCl? + 2NH?↑ + 2H?O。因此,銨態氮肥不能與堿性物質(如草木灰,主要成分K?CO?)混合施用。
檢驗方法:取少量樣品于試管中,加入氫氧化鈉溶液,微熱,將濕潤的紅色石蕊試紙靠近試管口。若試紙變藍,則證明含有NH??。
本題考點:銨鹽的性質、化肥的合理使用、NH??的檢驗。
三、 專題訓練及答案(部分)
訓練題1:如何鑒別氯化銨、硫酸銨和尿素【CO(NH?)?】三種氮肥?
答案要點:
1. 觀察狀態:尿素為白色顆粒狀,另兩種為晶體。
2. 取樣加入堿液并加熱,有氨味的是銨鹽(氯化銨和硫酸銨),無氨味的是尿素。
3. 向兩種銨鹽溶液中分別滴加硝酸鋇溶液,產生白色沉淀的是硫酸銨,另一種是氯化銨。
訓練題2:設計實驗證明某鉀肥(主要成分為K?SO?)中是否混入了NH?Cl。
答案要點:取少量樣品于試管中,加入氫氧化鈉溶液,微熱,用濕潤的紅色石蕊試紙檢驗生成的氣體。若試紙變藍,則證明混有NH?Cl;若不變藍,則未混入。
四、 與備考建議
1. 夯實基礎:牢記鹽的溶解性表、常見離子的檢驗方法、化肥的種類與特性。
2. 掌握方法:熟練掌握物質鑒別、分離、提純的實驗設計思路,步驟清晰,現象描述準確。
3. 聯系實際:關注化學知識與農業生產、環境保護的聯系,如化肥的合理施用、銨態氮肥的保存等。
4. 規范表達:化學方程式書寫規范,實驗表述嚴謹,避免因表述不清而失分。
通過以上系統性的專題訓練,結合對典型例題的深入剖析,考生能夠有效構建關于鹽和化肥的知識網絡,提升解決中考化學實驗探究類題目的能力,為取得優異成績奠定堅實基礎。自然科學的研究和試驗發展,正是建立在這樣嚴謹、求實的探究過程之上。